КРИСТАЛЛИЗАЦИЯ - утворення кристалів з газу, розчину, розплаву, скла або кристала ін. Структури (поліморфні перетворення). К. складається в укладанні атомів, молекул або іонів в кристалічну решітку . К. визначає освіту мінералів, льоду, грає важливу роль в атм. явищах, в живих організмах (утворення зубної емалі, кісток, ниркових каменів). Шляхом К. отримують і масивні монокристали, і тонкі кристалічні. плівки напівпровідників, діелектриків і металів. Масова К.- одночасним. зростання безлічі дрібних кристалів - лежить в основі металургії і широко використовується в хім., харчової та медичної промисловості.
Термодинаміка кристалізації. Розташування частинок в кристалі упорядковано (див. Далекий і близький порядок ), І їх ентропія SK менше ентропії Sc в невпорядкованою середовищі (парі, розчині, розплаві). Тому зниження темп-ри Т при пост. тиску р веде до того, що хімічний потенціал речовини в кристалі
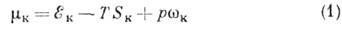
стає менше його потенціалу в вихідної середовищі:
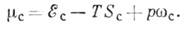
тут 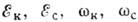 - енергії взаємодії частинок і уд. обсяг речовини в кристалічних. і неврегульованих станах (фазах), SK і SС - ентропії . Т. о., Кристалічні. фаза виявляється "вигідніше", відбувається К., супроводжувана виділенням т.зв. прихованої теплоти К .:
- енергії взаємодії частинок і уд. обсяг речовини в кристалічних. і неврегульованих станах (фазах), SK і SС - ентропії . Т. о., Кристалічні. фаза виявляється "вигідніше", відбувається К., супроводжувана виділенням т.зв. прихованої теплоти К .: 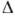 H = T (SC-SK)
H = T (SC-SK) 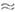 0,5-5 еВ, а також стрибком уд. обсягу
0,5-5 еВ, а також стрибком уд. обсягу 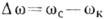 (Фазовий перехід першого роду). якщо р
(Фазовий перехід першого роду). якщо р  104 атм, то член
104 атм, то член 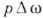 в співвідношенні (1) малий, і при
в співвідношенні (1) малий, і при 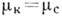 теплота К. дорівнює
теплота К. дорівнює 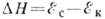 , Т. Е. Є мірою зміни енергії зв'язку між частинками при К. [при К. з розплаву
, Т. Е. Є мірою зміни енергії зв'язку між частинками при К. [при К. з розплаву 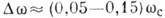 і може мати разл. знаки].
і може мати разл. знаки].
К. при поліморфних перетвореннях (див. поліморфізм ) Може бути фазовим переходом другого роду. У разі переходів першого роду межа розділу кристал - середовище локалізована в межах дек. міжатомних відстаней, і її уд. вільна енергія 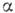 > 0.
> 0.
Для переходів 2-го роду межа не локалізована і
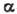 = 0.
= 0.
умови 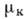 (Р, Т, Ск) =
(Р, Т, Ск) = 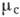 (Р, Т, Сс) для кожного з компонентів кристала і середовища визначають зв'язок р, Т і концентрації компонентів С, при яких кристал знаходиться в рівновазі з середовищем, т. Е. діаграму стану речовини. різниця
(Р, Т, Сс) для кожного з компонентів кристала і середовища визначають зв'язок р, Т і концентрації компонентів С, при яких кристал знаходиться в рівновазі з середовищем, т. Е. діаграму стану речовини. різниця 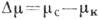 , Що є мірою відхилення від рівноваги, наз. термодінамі ч. рушійною силою К. Зазвичай вона створюється зниженням темп-ри нижче рівноважного значення Т0, тобто переохолодженням системи на
, Що є мірою відхилення від рівноваги, наз. термодінамі ч. рушійною силою К. Зазвичай вона створюється зниженням темп-ри нижче рівноважного значення Т0, тобто переохолодженням системи на 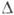 Т-Т0-Т. якщо
Т-Т0-Т. якщо
 Т
Т 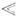 Т0, то
Т0, то

Якщо тиск р парів або концентрація С в розчині більше рівноважних значень р0 і С0, то говорять про абс. пересиченні ( 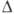 р = р - р0 або
р = р - р0 або  С = С-С0) або відносить. пересиченні (
С = С-С0) або відносить. пересиченні ( 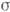 =
= 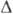 р / р0 або
р / р0 або  З / С0). В цьому випадку в розріджених парах і розлучених розчинах
З / С0). В цьому випадку в розріджених парах і розлучених розчинах
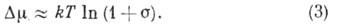
В процесі вирощування монокристалів з розчинів зазвичай 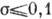 , З парів і при хім. реакціях
, З парів і при хім. реакціях 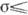 1, при конденсації молекулярних пучків
1, при конденсації молекулярних пучків 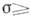 102-104.
102-104.
К. може відбуватися в результаті або за участю хім. реакцій. Рівноважний стан суміші газів при можливій хім. реакції між складовими її речовинами Ai можна узагальнено записати у вигляді 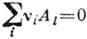 , де
, де 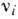 - стехіометріч. коеф. (
- стехіометріч. коеф. ( 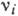 <0 для прямої реакції,
<0 для прямої реакції, 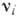 > 0 - для зворотного). В цьому випадку
> 0 - для зворотного). В цьому випадку
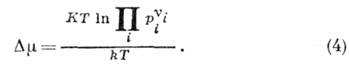
Тут К - константа рівноваги реакції, рi - парціальні тиску (Або концентрації, якщо реакція протікає в розчині). У разі електролітів

де Ze - заряд іона (Z - ат. номер), 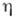 - відхилення різниці потенціалів між кристалом і розчином від рівноважного значення.
- відхилення різниці потенціалів між кристалом і розчином від рівноважного значення.
Зародки кристалізації. Пересичена або переохолоджених фаза може зберігати свій стан надзвичайно довго (К. не йде). Такий стан зв. метастабіл'ним. Розплави чистих металів переохолоджуватися на 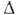 Т = (0,3-0,5) Т0, вода - на
Т = (0,3-0,5) Т0, вода - на 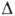 Т
Т 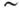 40 До
40 До 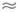 0,15 T0, пари - до s
0,15 T0, пари - до s 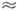 10, розчини - до
10, розчини - до 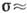 3. Скло можуть бути охолоджені до ОК (див. аморфний стан ) .Загрязнённие середовища кристалізуються на сторонніх частинках (центри К.) при невеликих
3. Скло можуть бути охолоджені до ОК (див. аморфний стан ) .Загрязнённие середовища кристалізуються на сторонніх частинках (центри К.) при невеликих 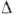 Т. Критич. переохолодження
Т. Критич. переохолодження 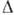 Т залежить також від темп-ри, матеріалу і стану стінок посудини, дії випромінювань. Причина такої стійкості - в труднощі зародження кристалів. Атоми і молекули газу або рідини можуть при зіткненнях з'єднуватися в агрегати з 2, 3 і т. Д. Частинок. Частина їх розпадається внаслідок флуктуації колебат. енергії частинок. Якщо кількість частинок N в агрегаті охоплює 2-4 координац. сфери, то до нього можна застосовувати макроскопіч. поняття поверхневої енергії і хім. потенціалу та ін. Ат. структура зародків поки недостатньо з'ясована. Однак є дані про те, що вона може відрізнятися від структури стійкої макроскопічної фази.
Т залежить також від темп-ри, матеріалу і стану стінок посудини, дії випромінювань. Причина такої стійкості - в труднощі зародження кристалів. Атоми і молекули газу або рідини можуть при зіткненнях з'єднуватися в агрегати з 2, 3 і т. Д. Частинок. Частина їх розпадається внаслідок флуктуації колебат. енергії частинок. Якщо кількість частинок N в агрегаті охоплює 2-4 координац. сфери, то до нього можна застосовувати макроскопіч. поняття поверхневої енергії і хім. потенціалу та ін. Ат. структура зародків поки недостатньо з'ясована. Однак є дані про те, що вона може відрізнятися від структури стійкої макроскопічної фази. 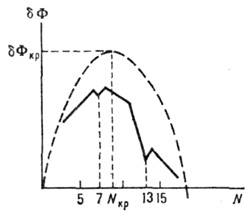
Мал. 1. Робота освіти зародка кристалізації 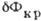 як функція числа частинок в ньому Nkp для феноменологічної (пунктир) і мікроскопічної (суцільна лінія) моделей.
як функція числа частинок в ньому Nkp для феноменологічної (пунктир) і мікроскопічної (суцільна лінія) моделей.
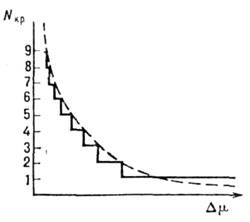
Мал. 2. Залежність числа частинок в критичному зародку Nkp від переохолодження для феноменологічної (пунктир) і мікроскопічної (суцільні лінії) моделей.
Переохолодження в однорідної гомогенної фазі визначається роботою освіти кордону розділу при появі кристалічної. фази всередині материнської. Ця робота позитивна, якщо питома вільна енергія кордону 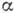 > 0. Освіта агрегату нової кристалічної. фази з N частинок з поверхнею
> 0. Освіта агрегату нової кристалічної. фази з N частинок з поверхнею 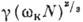 збільшує термодинамич. потенціал Ф системи на величину, рівну
збільшує термодинамич. потенціал Ф системи на величину, рівну 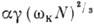 , Де число
, Де число 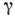 залежить від форми агрегату. Одночасно Ф зменшується на
залежить від форми агрегату. Одночасно Ф зменшується на 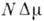 , Т. К. Нова фаза "вигідніше" старої
, Т. К. Нова фаза "вигідніше" старої 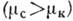 . В результаті робота освіти зародка
. В результаті робота освіти зародка 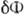 =
= 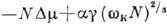 досягає максимуму
досягає максимуму 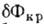 =
= 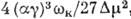 , Коли розмір зародка набуває критичного. значення Nkp =
, Коли розмір зародка набуває критичного. значення Nkp = 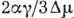 (Рис. 1). Робота освіти критич. зародка
(Рис. 1). Робота освіти критич. зародка 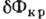 мінімальна для кристаликів рівноважної форми, у яких брало мінімальна поверхнева енергія при даному обсязі. Критич. зародки утворюються в результаті теплових флуктуації. Збільшення ступеня відхилення від рівноваги
мінімальна для кристаликів рівноважної форми, у яких брало мінімальна поверхнева енергія при даному обсязі. Критич. зародки утворюються в результаті теплових флуктуації. Збільшення ступеня відхилення від рівноваги 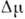 зменшує роботу освіти зародка. швидкість зародження
зменшує роботу освіти зародка. швидкість зародження
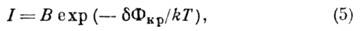
де В пропорційно щільності частинок в середовищі і швидкості їх приєднання до критичного. зародку (в очищених парах і розчинах В 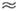 1025-1030 см-3с-1, в розплавах В
1025-1030 см-3с-1, в розплавах В 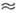 1037-1042 см-3 з-1). Число частинок в критич. зародку убуває з переохолодженням (в розплаві Ga при
1037-1042 см-3 з-1). Число частинок в критич. зародку убуває з переохолодженням (в розплаві Ga при 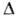 T = 0,5 Т0, Nkp
T = 0,5 Т0, Nkp 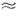 10 атомів, радіус зародка r3
10 атомів, радіус зародка r3 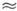 4 А). Т. к. Nkp не може змінюватися менше ніж на 1, то існують інтервали зміни
4 А). Т. к. Nkp не може змінюватися менше ніж на 1, то існують інтервали зміни 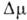 , В межах яких брало Nkp постійно (рис. 2). Ці інтервали малі в області помірних пересиченні, але проявляються при великих, напр. в умовах конденсації молекулярних пучків і електролітич. осадження, коли Nkp
, В межах яких брало Nkp постійно (рис. 2). Ці інтервали малі в області помірних пересиченні, але проявляються при великих, напр. в умовах конденсації молекулярних пучків і електролітич. осадження, коли Nkp 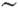 1-10. В результаті залежності
1-10. В результаті залежності 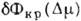 і I (
і I ( 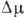 ) Стають ламаними лініями (рис. 1).
) Стають ламаними лініями (рис. 1).
До зародкам з дек. атомів поняття поверхневої енергії не може бути застосовано, і опис зародження ведеться на конкретних мікроскопіч. моделях. Однак для оцінок можна користуватися феноменологіч. уявленнями, що дають трохи занижену швидкість зародження (рис. 1, 2).
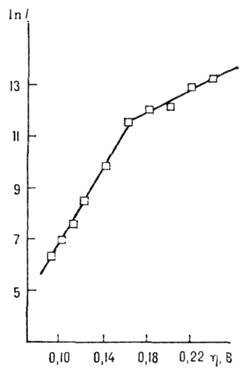
Мал. 3. Швидкість зародження In I на аморфному вуглеці при електролітичної кристалізації в залежності від перенапруги h: ліва пряма відповідає першому атому в зародку, права - другого.
Упаковка частинок в малих зародках може не збігатися з упаковкою в масивному кристалі, напр. виявлено дек. метастабільних фаз в краплях Ga і Вr, замерзлих при глибоких переохолодженнях. Мас-спектральний аналіз агрегатів в парах Pb і в Хе виявив підвищення вмісту кластерів з 7, 13, 19 і т. Д. Атомів, характерних для некрісталлографіч. пентагональними упаковки (рис. 4). Поверхневі атоми в цих кластерах утворюють завершену координац. сферу. Тому робота їх утворення мінімальна, а їх число максимально в порівнянні з зародками, що містять на 1 атом більше або менше.
Освіта зародка на добре смачиваемой поверхні кристала вимагає подолання меншого бар'єру, і тому таке гетерогенное зародження відбувається при менших переохолодженнях (див. Епітаксия ).

Мал. 4. Кристалографічна щільна (вгорі) і пентагональними (внизу) упаковки.
Зниження темп-ри не тільки зменшує роботу освіти зародка, але і експоненціально підвищує в'язкість розплаву, т. Е. Знижує частоту приєднання нових частинок до зародка (рис. 5, а). В результаті I ( 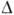 Т) спочатку досягає максимуму, а потім стає настільки малою (рис. 5, б), що при низьких темп-pax розплав твердне, залишаючись аморфним. У розплавах з порівняно малою в'язкістю це можливо лише при дуже швидкому (
Т) спочатку досягає максимуму, а потім стає настільки малою (рис. 5, б), що при низьких темп-pax розплав твердне, залишаючись аморфним. У розплавах з порівняно малою в'язкістю це можливо лише при дуже швидкому ( 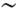 106 К / с) охолодженні. Так отримують аморфні сплави металів (див. аморфні метали ). У рідкому гелії освіту зародків можливо не переходом системи через бар'єр, а тунельним просочуванням крізь нього. При вирощуванні великих скоєних кристалів на "затравки" уникають появи спонтанних зародків, використовуючи слабо пересичені розчини або перегріті розплави. Навпаки, в металургії прагнуть отримати максимальну кількість центрів К., створюючи глибокі переохолодження (див. Нижче).
106 К / с) охолодженні. Так отримують аморфні сплави металів (див. аморфні метали ). У рідкому гелії освіту зародків можливо не переходом системи через бар'єр, а тунельним просочуванням крізь нього. При вирощуванні великих скоєних кристалів на "затравки" уникають появи спонтанних зародків, використовуючи слабо пересичені розчини або перегріті розплави. Навпаки, в металургії прагнуть отримати максимальну кількість центрів К., створюючи глибокі переохолодження (див. Нижче).
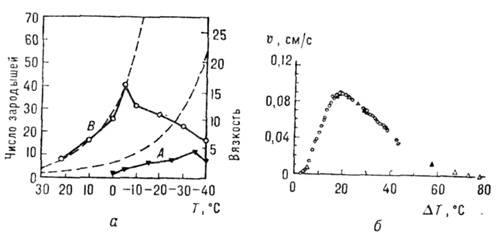
Мал. 5. Температурні залежності швидкості зародження і росту кристалу: а) суцільні криві - температурна залежність числа зародків цитринові кислоти в переохолоджених водному розчині (темп-ри насичення: А-62 ° С, В - 85 ° С); пунктир - збільшення в'язкості (в пуаз) розчинів з пониженням Т; б) швидкість росту v кристалів бензофенону з розплаву як функції  Т.
Т.
Зростання кристала може бути пошаровим і нормальним в залежності від того, чи є його поверхню в атомному масштабі гладкою або шорсткою. Атомні площини, що утворюють гладку грань, майже повністю укомплектовані і містять порівняно мало вакансій і атомів, адсорбованих в місцях, відповідних вузлів кристалічної. решітки наступного шару. Краї незавершених атомних площин утворюють ступені (рис. 6, в). В результаті теплових флуктуації щабель містить недо-рої число тривимірних входять кутів - зламів. Приєднання нової частинки до зламу не змінює енергії поверхні і тому є елементарним актом росту кристалу. Зі збільшенням відносини теплової енергії kT до поверхневої енергії 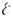 (В розрахунку на 1 атомне місце на поверхні) щільність зламів збільшується. Відповідно збільшується конфігураці. ентропія і падає вільна лінійна енергія ступені. При потужність. відносинах
(В розрахунку на 1 атомне місце на поверхні) щільність зламів збільшується. Відповідно збільшується конфігураці. ентропія і падає вільна лінійна енергія ступені. При потужність. відносинах 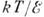 (близьких до 1, але кілька різних для різних граней) лінійна енергія ступені звертається в 0, і ступінь "розмазується" по межі, до-раю перетворюється в шорстку, т. е. рівномірно і щільно покриту зламами поверхню (рис. 6, б ). Зв'язок поверхневої енергії з теплотою К. дозволяє зробити висновок, що для речовин і темп-р, для яких брало зміна ентропії при К. таке, що
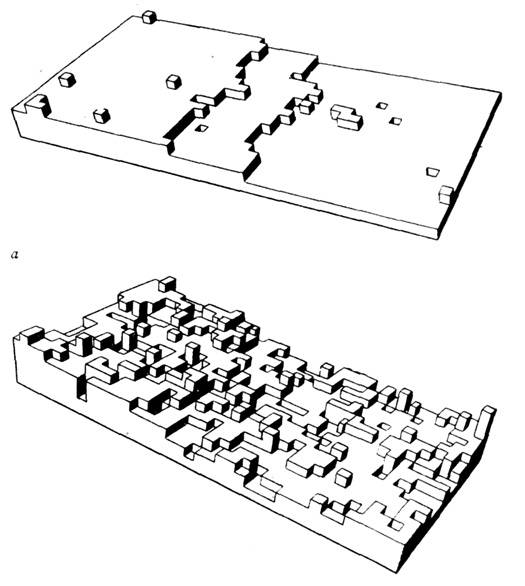
(близьких до 1, але кілька різних для різних граней) лінійна енергія ступені звертається в 0, і ступінь "розмазується" по межі, до-раю перетворюється в шорстку, т. е. рівномірно і щільно покриту зламами поверхню (рис. 6, б ). Зв'язок поверхневої енергії з теплотою К. дозволяє зробити висновок, що для речовин і темп-р, для яких брало зміна ентропії при К. таке, що 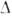 S / k> 4, все щільноупакована межі - гладкі. Ця ситуація характерна для рівноваги кристал - пар, а також (для деяких речовин) для кордону кристал -расплав. Перехід від шорсткості до огранений можливий при зміні концентрації в двокомпонентних системах (К. з розчинів). якщо
S / k> 4, все щільноупакована межі - гладкі. Ця ситуація характерна для рівноваги кристал - пар, а також (для деяких речовин) для кордону кристал -расплав. Перехід від шорсткості до огранений можливий при зміні концентрації в двокомпонентних системах (К. з розчинів). якщо 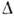 S / k <2 (типово для плавлення металів), то поверхні будь-якої орієнтації шорсткі. при
S / k <2 (типово для плавлення металів), то поверхні будь-якої орієнтації шорсткі. при 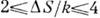 окремі гладкі грані співіснують з шорсткими поверхнями (напр., кристали Ge і Si в розплавах, гранати в розплавах і високотемпературних розчинах). Залежність вільної енергії і швидкості К. від орієнтації поверхні має гострі (сингулярні) мінімуми для гладких (сингулярних) граней і округлені (несінгулярние) для шорстких поверхонь.
окремі гладкі грані співіснують з шорсткими поверхнями (напр., кристали Ge і Si в розплавах, гранати в розплавах і високотемпературних розчинах). Залежність вільної енергії і швидкості К. від орієнтації поверхні має гострі (сингулярні) мінімуми для гладких (сингулярних) граней і округлені (несінгулярние) для шорстких поверхонь.
Мал. 6. Атомно-гладка (а) і шорстка (б) поверхні (моделювання на ЕОМ).

Мал. 7. Концентричні ступені на межі (100) NaCl при зростанні з молекулярного пучка. Висота щабля 2,82 А (декоровані дрібними кристалами спеціально обложеного золота).

Мал. 8. а - Спіральна форма зростання; б - ступінь, що закінчується на поверхні в точці її перетину гвинтової дислокацією .
Приєднання нового атома в будь-якому положенні на поверхні крім зламу змінює її енергію. Заповнення нечисленних вакансій, що знижує цю енергію, не може дати початку нового атомного шару, а концентрація атомів в місцях, відповідних вузлів решітки наступного шару, підвищує енергію і тому мала. В результаті необоротне приєднання частинок до кристалу, т. Е. Його зростання, можливий тільки коли на його поверхні є злами. На шорсткуватих поверхнях щільність зламів велика, і зростання вздовж нормалі до поверхні можливий практично в будь-якій точці. Таке зростання зв. нормальним. Він лімітується швидкістю приєднання отд. частинок до зламів. Його швидкість R лінійно збільшується з переохолодженням на фронті К .:
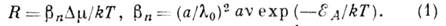
Тут а - міжатомних відстань, l0 - відстань між зламами, 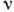 - ефективна частота теплових коливань ,
- ефективна частота теплових коливань , 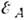 - енергія, необхідна для приєднання частинок до зламу (енергія активації). Вона враховує перебудову ближнього порядку в рідини, десольватації будує. частинок і зламів в розчинах, хім. реакції і т. д. У простих розплавах коеф.
- енергія, необхідна для приєднання частинок до зламу (енергія активації). Вона враховує перебудову ближнього порядку в рідини, десольватації будує. частинок і зламів в розчинах, хім. реакції і т. д. У простих розплавах коеф. 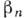 великі, що забезпечує зростання з помітною швидкістю, коли переохолодження на фронті К.
великі, що забезпечує зростання з помітною швидкістю, коли переохолодження на фронті К. 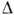 Т
Т 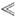 1 К. Так, для росту Si
1 К. Так, для росту Si 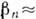 106 см / с R = (3-5) * 10-3 см / с досягається при
106 см / с R = (3-5) * 10-3 см / с досягається при 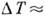 10-5 К. При досить низьких темп-pax рухливість частинок падає і швидкість росту зменшується, подібно швидкості зародження (рис. 5, б).
10-5 К. При досить низьких темп-pax рухливість частинок падає і швидкість росту зменшується, подібно швидкості зародження (рис. 5, б).
Якщо поверхня гладка, то злами існують тільки на ступенях, зростання йде последоват. відкладенням верств і зв. пошаровим. Якщо поверхня утворена сходами однакових ступенів і в середньому відхилена від найближчої сингулярной межі на кут з тангенсом р, то пор. швидкість її зростання вздовж нормалі до цієї сингулярной орієнтації

де 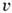 - швидкість росту ступені уздовж межі,
- швидкість росту ступені уздовж межі, 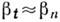 (В розчинах
(В розчинах 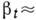 10-1-10-3 см / с.)
10-1-10-3 см / с.)
Щільність ступенів визначається тим, генеруються вони двовимірними зародками або дислокациями .Образованіе двовимірних зародків вимагає подолання потенційного бар'єру, висота к-якого пропорційна лінійної енергії ступенів і обернено пропорційна 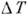 . Відповідно, швидкість К. експоненціально мала при малих
. Відповідно, швидкість К. експоненціально мала при малих 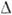 Т [для росту грані (III) Si з R = (3-5) * 10-3 см / с необхідно
Т [для росту грані (III) Si з R = (3-5) * 10-3 см / с необхідно 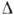 Т
Т 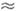 0, ЗК; див. вище]. При К. з молекулярних пучків, якщо є місця переважного освіти двовимірних зародків, щаблі мають вигляд замкнутих кілець (рис. 7). Можливо, що утворення зародків "полегшується" точками виходу на поверхню крайових дислокацій.
0, ЗК; див. вище]. При К. з молекулярних пучків, якщо є місця переважного освіти двовимірних зародків, щаблі мають вигляд замкнутих кілець (рис. 7). Можливо, що утворення зародків "полегшується" точками виходу на поверхню крайових дислокацій.
При зростанні на гвинтовий дислокації, утворена нею щабель в процесі росту набуває спіральну форму (рис. 8), т. К. В точці закінчення ступені на дислокації її швидкість росту дорівнює 0. У процесі спірального зростання новий шар "накручується" сам на себе навколо точки виходу дислокації і на поверхні виникає пологий (віцінальним) горбок зростання. Часто горбки утворюються групою дислокацій, сумарний вектор Бюргерса яких брало має в напрямку нормалі до поверхні складову Ь, рівну дек. параметрам а решітки. Точки виходу цих дислокацій можуть займати на поверхні деяку область (з периметром 2L, рис. 9, а, в). В цьому випадку схил кругового віцінальним горбка утворює з сингулярної гранню кут з тангенсом р = b / (19rc +2 h) (рис. 9, б). Нахили горбків вимірюються 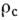 методами оптич. интерферометрии (Рис. 10), методом квітів тонких пластинок, а іноді безпосередньо візуалізацією ступенів.
методами оптич. интерферометрии (Рис. 10), методом квітів тонких пластинок, а іноді безпосередньо візуалізацією ступенів.
-
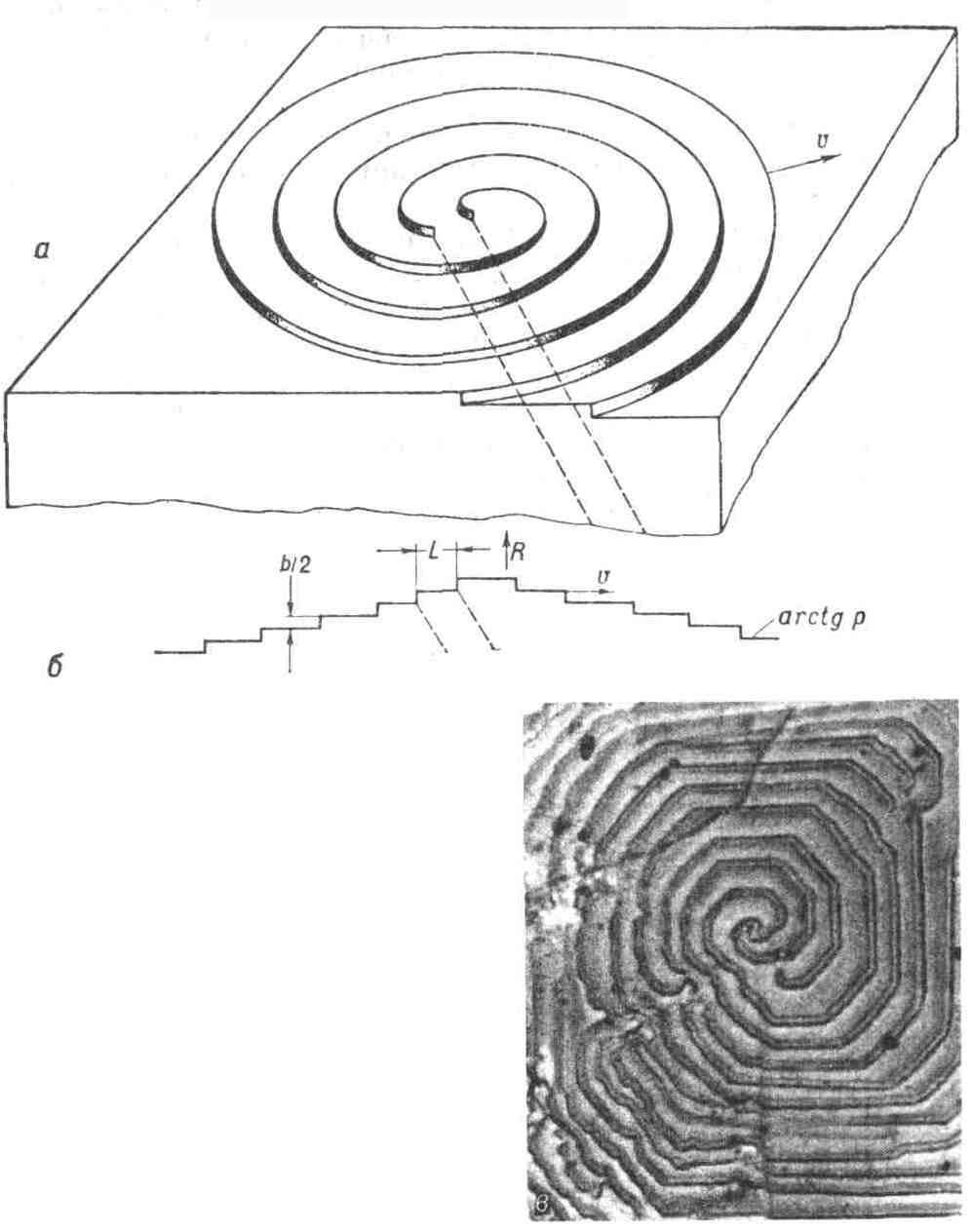
Мал. 9. двухзаходная спіраль, яка утворює віцінальним горбок навколо точок виходу на поверхню двох дислокацій: о) загальний вигляд горбка; б) його перетин площиною, перпендикулярної грані і проходить через точки виходу дислокацій; в) спіраль на межі (100) синтетичного алмазу. 
Мал. 10. Інтерференційні смуги від віцінальним горбка на грані призми кристала ADP (зростання з водного розчину).
Радіус двовимірного крітяч. зародка 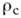 пропорційний лінійної енергії ступені і обернено пропорційний
пропорційний лінійної енергії ступені і обернено пропорційний  Т. Тому зі збільшенням
Т. Тому зі збільшенням 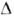 Т крутизна горбка р лінійно збільшується при малих
Т крутизна горбка р лінійно збільшується при малих  Т і прагне до насичення при великих (при L
Т і прагне до насичення при великих (при L 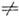 0). Відповідно, нормальна швидкість росту R квадратично збільшується з пересиченням
0). Відповідно, нормальна швидкість росту R квадратично збільшується з пересиченням 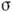 при малих переохолодженнях і лінійно - при великих (рис. 11). Варіації вектора Бюргсрса і протяжність L дислокації. джерела визначають розкид значень швидкості росту кристалографічна ідентичних граней (або однієї і тієї ж межі) в однакових умовах. В процесі зростання межі точка виходу не перпендикулярній їй дислокації зміщується і може досягти одного з ребер. Після цього ступінь зникає. Далі К. йде лише шляхом двовимірного зародження, і швидкість росту при малих переохолодженнях падає (принаймні в дек. Раз при К. з розплаву і на дек. Порядків при К. з розчину). Через відносно малих значень лінійної енергії ступенів на кордоні кристал - розплав і фактично усувають проблему доставки речовини, що кристалізується
при малих переохолодженнях і лінійно - при великих (рис. 11). Варіації вектора Бюргсрса і протяжність L дислокації. джерела визначають розкид значень швидкості росту кристалографічна ідентичних граней (або однієї і тієї ж межі) в однакових умовах. В процесі зростання межі точка виходу не перпендикулярній їй дислокації зміщується і може досягти одного з ребер. Після цього ступінь зникає. Далі К. йде лише шляхом двовимірного зародження, і швидкість росту при малих переохолодженнях падає (принаймні в дек. Раз при К. з розплаву і на дек. Порядків при К. з розчину). Через відносно малих значень лінійної енергії ступенів на кордоні кристал - розплав і фактично усувають проблему доставки речовини, що кристалізується 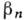 ,
, 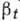 і Л на дек. порядків вище, ніж для К. з розчинів і газової фази.
і Л на дек. порядків вище, ніж для К. з розчинів і газової фази.
Зважаючи на малу щільності газової фази послойная К. з неї йде в осн. не прямим попаданням частинок на ступені, а за рахунок дифузії частинок, адсорбованих на атомно-гладких "терасах" між ступенями. За час між моментами прилипання до поверхні і десорбції така частка робить випадкові блукання по поверхні і йде від точки прилипання на відстань близько пор. довжини дифузійного пробігу ls. Тому досягти ступені можуть лише частки, адсорбована навколо неї в смузі шириною 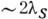 Більшість частинок, що падають на поверхню з малою щільністю ступенів, випаровуються - коеф. конденсації для таких поверхонь малий. Він наближається до 1 при великій щільності ступенів, т. Е. При значить. пересиченнях. З тієї ж причини швидкість К. з газової фази навіть на одній дислокації квадратично збільшується з пересиченням при малих пересиченнях і лінійно - при великих. При конденсації молекулярних пучків ступені утворюються шляхом двовимірного зародження в місцях, де пересичення в адсорбционном шарі досягає критичного, і тому пор. відстань між ступенями визначається довжиною пробігу адсор-бирів. частинок.
Більшість частинок, що падають на поверхню з малою щільністю ступенів, випаровуються - коеф. конденсації для таких поверхонь малий. Він наближається до 1 при великій щільності ступенів, т. Е. При значить. пересиченнях. З тієї ж причини швидкість К. з газової фази навіть на одній дислокації квадратично збільшується з пересиченням при малих пересиченнях і лінійно - при великих. При конденсації молекулярних пучків ступені утворюються шляхом двовимірного зародження в місцях, де пересичення в адсорбционном шарі досягає критичного, і тому пор. відстань між ступенями визначається довжиною пробігу адсор-бирів. частинок.
Підведення Речовини до зростаючої поверхні и відведення від неї теплоти К. обмежує ШВИДКІСТЬ К., коли ЦІ процеси протікають повільніше поверхнево. Такий діфузійній режим типів для К. з розплавів и неперемешіваемій розчінів. Висока швидкість К. з розплаву лежить в основі всіх широко використовуваних методів вирощування монокристалів, в яких брало швидкість К. задається механічні. рухом кристала відносно незалежно формованого теплового поля. Кинетич. режим К., коли швидкість К. лімітується поверхневими процесами, характерний для К. з перемішуються розчинів, з газової фази і зростання з перемішуваного розплаву кристалів з високою ентропією плавлення.
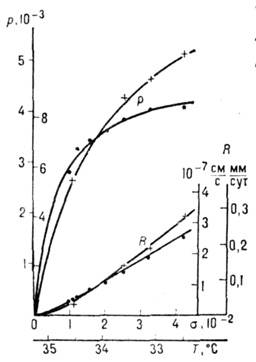
Мал. 11. Нахили р віцинальних горбків, утворених двома різними дислокаційними джерелами, і задаються ними швидкості росту грані R в залежності від пересичення 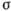 .
.
Форми росту кристалів (габітус) визначаються анізотропією швидкості К. і умовами тепло- і масопереносу. Кристали з шорсткими поверхнями мають зазвичай округлу форму. Атомно-гладкі поверхні проявляються у вигляді граней. Стаціонарна форма кристалічної. багатогранника така, що відстань від центру до кожної грані пропорційно її швидкості росту. В результаті кристал виявляється утвореним гранями з хв. швидкостями росту (межі з великими швидкостями поступово зменшуються і зникають). Вони паралельні площинам з наиб. щільною упаковкою і наиб. сильними зв'язками в атомній структурі кристала. Тому кристали з цепочечной і шаруватою структурою мають игольчатую або таблитчатих форму. Анізотропія швидкостей росту і, отже, форма росту кристалу в разл. фазах залежать від складу, Т, 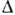 Т і сильно змінюються під дією поверхнево-активних домішок.
Т і сильно змінюються під дією поверхнево-активних домішок.
Через великий швидкості поверхневих процесів К. переохолодження  Т на атомно-шорсткуватих поверхнях мало, т. Е. Т = Т0 (звідси назв. Ізотерми). Щільноупакована межі з простими індексами в разі неметалів часто залишаються сингулярними і з'являються на округлому фронті К. у вигляді плоского зрізу в формі кола, еліпса або кільця (рис. 12, а) в залежності від форми ізотерми К. Темп-ра уздовж такої грані не постійна і досягає мінімуму в точках, наиб. віддалених від ізотерми Т = Т0. У цих точках найвищого переохолодження генеруються шари, що визначають швидкість росту грані. Тому стаціонарний розмір межі тим більше, чим більша
Т на атомно-шорсткуватих поверхнях мало, т. Е. Т = Т0 (звідси назв. Ізотерми). Щільноупакована межі з простими індексами в разі неметалів часто залишаються сингулярними і з'являються на округлому фронті К. у вигляді плоского зрізу в формі кола, еліпса або кільця (рис. 12, а) в залежності від форми ізотерми К. Темп-ра уздовж такої грані не постійна і досягає мінімуму в точках, наиб. віддалених від ізотерми Т = Т0. У цих точках найвищого переохолодження генеруються шари, що визначають швидкість росту грані. Тому стаціонарний розмір межі тим більше, чим більша  Т потрібно для її зростання зі швидкістю, що дорівнює швидкості округлого фронту К. в напрямку витягування кристала. Шорсткі і гранниє поверхні захоплюють різні кол-ва домішок, і кристал з сосуществующими гранями і шорсткими формами виростає неоднорідним (рис. 12, б).
Т потрібно для її зростання зі швидкістю, що дорівнює швидкості округлого фронту К. в напрямку витягування кристала. Шорсткі і гранниє поверхні захоплюють різні кол-ва домішок, і кристал з сосуществующими гранями і шорсткими формами виростає неоднорідним (рис. 12, б).
Мал. 12. Освіта плоскій грані на округлому фронті кристала (кристал витягується з розплаву): а - осьовий переріз кристала з фронтом кристалізації, увігнутим в сторону кристала в центрі і плоским по периферії; б -продольное перетин кристала Si (периферич. область збагачена домішками).
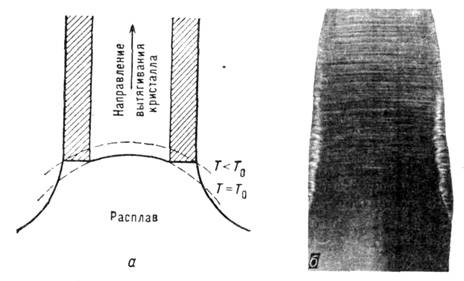
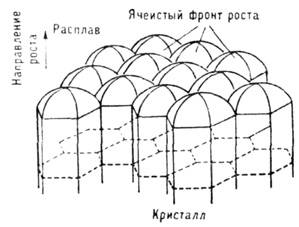
Якщо Т в розплаві зменшується в міру віддалення від фронту К., то фронт нестійкий: випадково що виник на ньому виступ потрапляє в область більшого переохолодження, швидкість росту вершини виступу стає ще більше і т. Д. В результаті плоский фронт розпадається на прилеглі один до одного пластинчасті або голчасті кристали - в перерізі, паралельному фронту, виникає полосчатая або чарункова структура. Осередки характерні для великих градієнтів темп-ри і мають зазвичай гексагональную форму незалежно від симетрії кристала (рис. 13). Нестійкість не сумісна з вирощуванням досконалих монокристалів, т. К. Веде до захоплення включень маткової середовища. Сферич. кристал, що росте в переохолоджених розплаві або розчині, зберігає свою форму, поки його радіус не досягне критичного. значення, що залежить від радіуса критич. зародка і швидкості поверхневих процесів К. Надалі розвиваються виступи, і кристал набуває кісткову (рис. 14, а, б) або дендритну форму (рис. 14, в, г). Назва останньої пов'язується з появою вторинних гілок після досягнення первинним виступом критич. Довжина.
Мал. 13. Схема пористої структури фронту кристалізації.
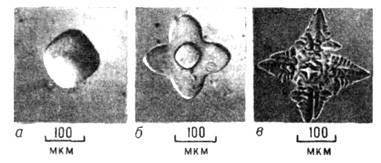
Мал. 14. Вихідний округлий кристал циклогексанолу в розплаві (а), початкова стадія зростання скелетного кристала (б), дендрит (в), дендрит при великому переохолодженні (г).
Домішка, відштовхує фронтом К. з розплаву, накопичується перед ним і, змінюючи рівноважну темп-ру К., викликає т. Н. концентрац. переохолодження, збільшується в міру віддалення від фронту. Якщо рівноважна темп-pa в розплаві збільшується з відстанню від фронту швидше, ніж справжня, то виникає концентраційна нестійкість. Вона зникає при досить високих відносинах градієнта темп-ри на фронті К. до його швидкості.
Фронт К. з розчину завжди нестійкий, т. К. Пересичення 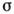 збільшується в міру віддалення від зростаючої поверхні. Для огранованих кристалів характерна велика пересичення близько вершин і ребер, причому перепад
збільшується в міру віддалення від зростаючої поверхні. Для огранованих кристалів характерна велика пересичення близько вершин і ребер, причому перепад 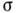 збільшується з розміром грані. При досить великих пересичені-ванні і розмірі межі вершини стають провідними джерелами ступенів зростання, а в центр. частинах граней виникають провали - починається скелетний ріст (рис. 15). Йому сприяють нек-риє домішки. Нестійкість К. з розчинів пригнічується інтенсивним перемішуванням, зниженням пересичення, а іноді введенням домішок.
збільшується з розміром грані. При досить великих пересичені-ванні і розмірі межі вершини стають провідними джерелами ступенів зростання, а в центр. частинах граней виникають провали - починається скелетний ріст (рис. 15). Йому сприяють нек-риє домішки. Нестійкість К. з розчинів пригнічується інтенсивним перемішуванням, зниженням пересичення, а іноді введенням домішок.

Мал. 15. Структурний кристал шпінелі.
Захоплення домішок. Ставлення концентрацій домішки в кристалі і вихідну речовину зв. коеф. захоплення До. При К <1 К. веде до очищення від домішки кристала, при К> 1 - до очищення вихідної середовища, К = 1 відповідає збереженню концентрації. Коеф. захоплення різними гранями різні і не збігаються з Термодім-наміч. рівноважними, обумовленими діаграмою стану. Тому склад кристала відхиляється від термодинамічно рівноважного. Так, при лазерної або електронною імпульсною рекристалізації тонких приповерхневих шарів Si зі швидкостями К. до дек. м / с концентрація домішок As, Sb, In, Bi в кристалі Si перевершує рівноважну в 3-600 разів, причому переважна більшість домішкових атомів знаходиться в вузлах решітки. Це пов'язано, по-перше, зі статистич. відбором: кожен вузол решітки при К. остаточно заповнюється тим чи іншим атомом після безлічі спроб (від 106-107 при швидкостях 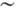 10-3 см / с і до 10 при швидкостях
10-3 см / с і до 10 при швидкостях 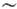 м / с). По-друге, в умовах швидкої К. не встигає протікати дифузія в розплаві.
м / с). По-друге, в умовах швидкої К. не встигає протікати дифузія в розплаві.
Нерівноважний захоплення домішки при пошаровому зростанні пов'язаний зі статистич. відбором на щаблях, а також з тим, що навіть рівноважна концентрація домішки в поверхневому шарі кристала і торці ступені помітно відрізняється від об'ємної. При досить швидкому відкладення шарів наступний шар замуровує попередній разом з міститься в ньому домішкою. В результаті кожна грань захоплює домішка в кол-ве, що відповідає концентрації в її поверхневому шарі, і кристал виявляється складеним з секторів зростання різних граней, з разл. концентраціями домішок і ін. дефектів - виникає т. Н. секторіальноє будова кристала (рис. 16). Кількість домішки, захоплює при русі ступені по межі, залежить від орієнтації цьому ступені. Тому сектор зростання даної межі, в свою чергу, розбивається на області, відкладені віціналямі різної орієнтації з різним вмістом домішки (віцінальним секторіальних, рис. 17).
Темп-pa і концентрація домішки на фронті К. з розплаву флуктуируют через конвекції розплаву і обертання кристала і тигля в зазвичай злегка несиметричному тепловому полі. Відповідні положення фронту К. друкуються в кристалі у вигляді смуг (Зонар-ве будова, рис. 16). Флуктуації темп-ри можуть бути настільки сильні, що зростання кристала змінюється плавленням і пор. швидкість виявляється на порядок менше миттєвою. Інтенсивність конвекції і амплітуда полосчатости зменшуються при вирощуванні кристалів у невагомості.

Мал. 16. секторіальних і занурені будова кристала алюмокалієвих квасцов.
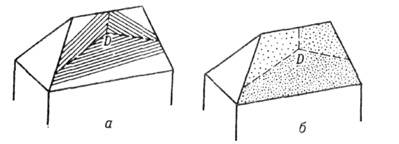
Мал. 17. віцінальним горбок, утворений на межі ступенями трьох різних орієнтації навколо крайової дислокації D (a). Різні схили пагорба захоплюють різні кількості домішки (б).
Освіта дефектів. Сторонні гази, розчинні в розчинах і розплавах краще, ніж в кристалах, виділяються на фронті К. Бульбашки газу захоплюються зростаючим кристалом, якщо вони перевищують критичного. розмір, регресний зі збільшенням швидкості росту (аналогічно захоплюються тверді частинки). При К. в невагомості конвективний відведення бульбашок від фронту К. утруднений і кристал збагачується газовими включеннями. Спеціально створюючи бульбашки, отримують піноматеріали. Реальні кристали завжди мають занурені і секторіально розподілені домішки, к-які змінюють параметр решітки, що викликає внутр. напруги, дислокації і тріщини. Останні виникають також через невідповідність параметрів решіток затравки (підкладки) і наростаючого на ній кристала. Джерелами внутр. напруг і дислокацій є також включення маткової середовища і сторонніх часток.
При К. з розплаву дислокації виникають через термопружних напруг, викликаних нелінійним розподілом темп-ри; при охолодженні вже виросли частин кристала зовні; при лінійному розподілі темп-ри уздовж нормалі до досить протяжна фронту К., якщо вільний температурний вигин кристала неможливий; успадкуванням з затравки. Тому вирощування бездислокаційних кристалів Si, GaAs, IP починають з запалів малого діаметра і ведуть в максимально однорідному температурному нулі. Кристали можуть містити петлі дислокацій розміром менше 1 мкм. Петлі утворюються як контури дископодібних скупчень (кластерів) міжвузлових атомів (або вакансій), що виникли в результаті розпаду пересиченого твердого розчину при охолодженні виріс кристала. Атоми домішки можуть бути центрами зародження кластерів.
Масова До. При потужність. умовах можливий одночасним. зростання безлічі кристалів. Спонтанне масова поява зародків і їх зростання відбуваються, напр., При затвердінні відливок металів. Кристали зароджуються насамперед на охолоджуваних стінках виливниці, куди заливається перегрітий метал. Зародки на стінках орієнтовані хаотично, проте в процесі росту "виживають" ті з них, у яких брало напрямок макс. швидкості росту перпендикулярно стінці (геометричний. відбір кристалів). В результаті у поверхні виникає т.зв. столбчатая зона, що складається з вузьких кристалів, витягнутих уздовж нормалі до поверхні.
Масова К. в розчинах починається або на спонтанно виникли зародках, або на спеціально введених затравки. Стикаючись в перемішувати розчині між собою, зі стінками посудини і мішалкою, кристалики руйнуються і дають початок новим центрам К. (вторинне зародження). Причиною вторинного зародження можуть бути також дрібні уламки нависають над гранню шарів, "запечатувальних" плоскі паралельні грані, включення маточного розчину. У металургії використовують сильні конвективні потоки, обламують дендритні кристали і розносять центри К. по всьому об'єму, іноді застосовують УЗ-дроблення зростаючих кристалів. Масової К. очищають речовини від домішки (К <1). Масова К. з газової фази (в т. Ч. З плазми) використовується для отримання ультрадисперсних порошків з розмірами кристалів до 10-6 см і менше. Необхідні для цього високі переохолодження досягаються різким охолодженням пара суміші хімічно реагуючих газів або плазми. Відомий спосіб масової К. крапель, що кристалізуються під час падіння в охолоджуваному газі.
Літ .: Вирощування кристалів з розчинів, 2 вид., Л., 1983; Леммлейн Г. Г., Морфологія і генезис кристалів, М., 1973; Лодіз Р. А., Паркер Р. Л., Зростання монокристалів, пров. з англ., М., 1974; Проблеми сучасної кристалографії, М., 1975; Сучасна кристалографія, т. 3, М., 1980; Чернов А. А., Фізика кристалізації, М., 1983; Гегузін Я. Е., Kаганевскій Ю. С., Дифузійні процеси на поверхні кристала, М., 1984; Морохов І. Д., Трусов Л. І., Лаповок Яків Семенович В. Н., Фізичні явища в ультрадисперсних середовищах, М., 1984; Скрипів В. П., Коверда В. П., Спонтанна кристалізація переохолоджених рідин, М., 1984.
А. А. Чернов.
покажчик >>

